研究内容のご紹介
Pheochromocytoma/Paraganglioma
1)はじめに
褐色細胞腫(Pheochromocytoma)は、交感神経節由来の腫瘍で副腎髄質に発生する。特に副腎髄質以外の傍神経節から発生する腫瘍を傍神経節腫(Paraganglioma)と呼ぶ。
Pheochromocytoma/Paragangliomaは30~40%と遺伝性の頻度が極めて高いといわれており、かつ15種類の原因遺伝子が同定されている。
褐色細胞腫の原因になりうる主要15遺伝子
| NF1 | RET ○ | VHL ○ | SDHA ○(NGS) | SDHB ○ |
| SDHC ○ | SDHD ○ | SDHAF2 ○(NGS) | TMEM127 ○ | MAX ○ |
| HIF2A | KIF1B | PHD2 | HRAS | FH |
○印:本研究室で解析可能な遺伝子
2)10%ルールは本当か?
褐色細胞腫は10%病と呼ばれる。すなわち10%は、遺伝性・両側・副腎外・悪性というものである。
2014年の米国内分泌学会のPPGL診断・治療ガイドラインにおいて200例以上の症例を集めた論文のメタ解析が行なわれ、遺伝性の頻度は33.8%(1250/3694)と報告された。
2007年から2015年までにおける本研究室での解析結果では、発端者178例中遺伝子変異陽性は66例であり、変異陽性率は37.1%であった。
すなわち、有名な‘褐色細胞腫の10%ル-ル’は、遺伝性の頻度に関しては明らかに過少評価である。

また、その内訳はSDHB. 31例,SDHD. 7例,SDHA. 1例,VHL. 14例,RET.4例,TMEM127. 4例,MAX. 5例)であり、SDHB. 31例中13例(41.9%)は悪性例であった。
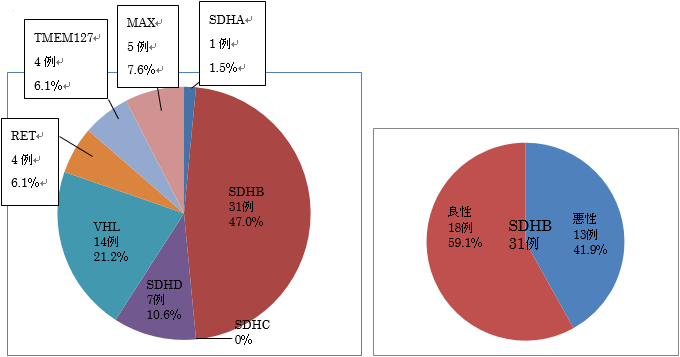
178例中41例が悪性褐色細胞腫であり、その内17例(41.5%)で変異が認められた。
17例中13例(76.5%)はSDHB遺伝子であった。
悪性褐色細胞腫における遺伝子変異の内訳

- SDHB n=13
- MAX n=1
- SDHD n=1
- VHL n=1
- RET n=1
- TMEM127 n=0
遺伝子変異で引き起こされる褐色細胞腫・パラガングリオーマの全体を指して遺伝性褐色細胞腫・パラガングリオーマ症候群(Hereditary pheochromocytoma/paraganglioma syndrome:HPPS)と呼ぶ。
また、Pheochromocytoma and Paragangliomaを以下PPGLと省略する。
3)原因遺伝子について
HPPSの原因のひとつにコハク酸脱水素酵素(複合体Ⅱ)の遺伝子異常がある。コハク酸脱水素酵素(複合体Ⅱ)は4つのサブユニット(Fp、Ip、cyb L、cyb S)で構成される。
コハク酸脱水素酵素サブユニットについて
| 遺伝子(サブユニット) | 遺伝子座 | 補因子(補欠分子族) | 生殖細胞変異で発症する患者 |
| SDHA (Fp) | 5p15 | FAD |
Leigh脳症 |
| SDHB (Ip) | 1p35 | 鉄‐硫黄タンパク | Paraganglioma |
| SDHC (cyb L) | 1q23 | Heme b | Paraganglioma |
| SDHD (cyb S) | 11q23 | Heme b | Paraganglioma |
SDHxの変異によるHPPSは、それぞれ変異遺伝子により特徴的な臨床像を呈する。例えば、SDHBの変異によるHPPSは、腹部のパラガングリオーマを初発部位としその後高率に遠隔転移つまり悪性化を引き起こす。また、SDHDの変異は頭頸部の多発性パラガングリオーマを起こしやすいが、悪性化の頻度は0~7%と低い。
その他のHPPSの原因遺伝子について
|
TMEM127 |
mTORの活性を負に制御している膜タンパクをコードしている遺伝子 |
|
MAX |
mTORの活性制御に関係している |
|
FH |
フマラーゼをコードしている遺伝子 |
腫瘍細胞における体細胞遺伝子変異による発症も、全症例の15~20%に報告されている。内訳は、NF-1、VHL、RET、MAXの体細胞遺伝子変異が多い。また、HIF2A、HRASの体細胞遺伝子変異も報告されている。
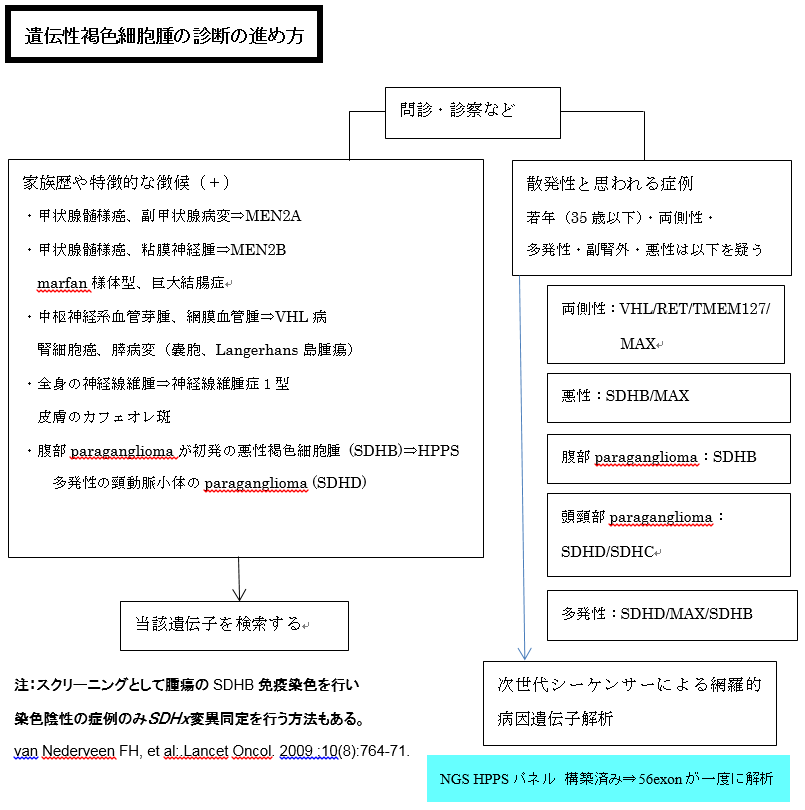
4)遺伝子検査について
本邦においても遺伝性は40%近くと高率で、さらにSDHB変異例は悪性化と密接に関連することが初めて証明された(投稿準備中)。
今後更に遺伝子診断(遺伝学的検査)の重要性は増すと考えられる。本研究室においては、サンガーシーケンスと次世代シーケンサー(NGS)で、現在検査を実施している。変異が認められた場合には、in silico解析を行っている。
5)発症機序について
遺伝子変異によりコハク酸脱水素酵素(複合体Ⅱ)の機能低下を来すことがPPGL発症を招く。ただし、このような代謝異常と発がんを結びつける機序は長い間missing rinkとされ不明であった。
我々は最近、in vitroの系で下記のようにその機序の一端を明らかにしている。
Saito Y, Ishii KA, Aita Y, Ikeda T, Kawakami Y, Shimano H, Hara H, Takekoshi K. Loss of SDHB elevates catecholamine synthesis and secretion depending on ROS production and HIF stabilization. Neurochem Res. 2016 Apr;41(4):696-706.
我々はラットの褐色細胞腫細胞PC12において、SDHB遺伝子をノックダウン(KD)することで、コハク酸脱水素酵素(複合体Ⅱ)活性が極めて低い(5%以下)実験系を確立した。

活性酸素(ROS)増加によりHIF-1αが活性化され、HIF-1α依存性にカテコ―ルアミン合成・分泌亢進、アポト―シス抵抗性が起こる事を明らかにしている。
すなわち本論文ではSDHBノッダウンでTCA回路のコハク酸脱水素酵素活性を低下させると腫瘍形成に至ることが示された。
6)今後について
遺伝性の頻度が高い点と変異遺伝子毎に臨床症状が異なる点を勘案すると、本疾患は遺伝情報を用いたオーダーメイド医療を考慮すべき疾患であり、今後そのロールモデル的役割を担うことが期待される。
分子標的薬の作用機序がさらに解明され、遺伝子診断を用いた症例ごとの個別化が可能になれば、最適な分子標的薬を選択することで、副作用だけでなく適切な投与量や期待される効果も正確に判定できるようになるはずである。
したがって、褐色細胞腫における適切な遺伝子診断は患者と家族にとって有用であり、かつ医科学の進展にもさらに貢献するものと思われる。
一方で、遺伝学的検査には常に細心の倫理的な配慮が必要である。
※遺伝子検査に関するご相談は下記、竹越一博までお問い合わせください。
お問い合わせ先:
〒305-8577
茨城県つくば市天王台1-1-1 医学系学系棟235
筑波大学 医学医療系 臨床検査医学/スポーツ医学 竹越一博
電話:029-853-3389
Eメール:k-takemd*md.tsukuba.ac.jp
Eメールを送信する際は*を@に変えてください。
 臨床検査医学
臨床検査医学